| 恒瑞SHR4640启动临床III期,进军国内痛风和降尿酸市场 | 您所在的位置:网站首页 › 降尿酸安全药物 › 恒瑞SHR4640启动临床III期,进军国内痛风和降尿酸市场 |
恒瑞SHR4640启动临床III期,进军国内痛风和降尿酸市场
|
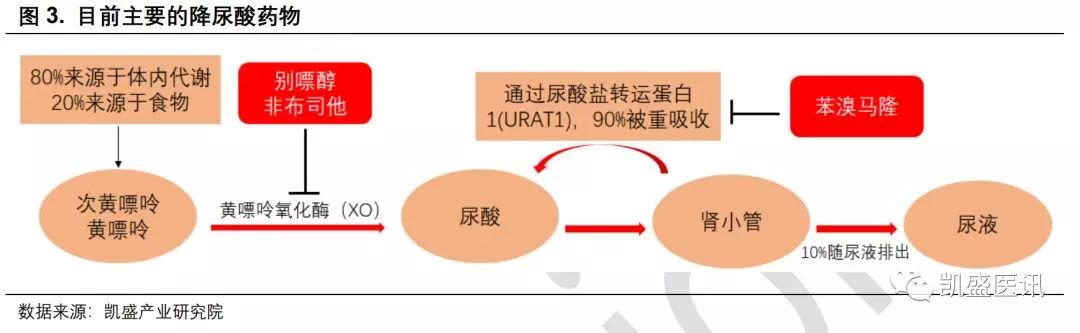
目前主要的降尿酸药物存在其局限性 目前的降尿酸药物可分为两类,一类为抑制尿酸合成药物,包括别嘌醇和非布司他,通过抑制黄嘌呤氧化酶的活性,减少尿酸的合成,降低血尿酸水平;另一类属于促尿酸排泄药,主要产品为苯溴马隆,通过抑制尿酸盐转运蛋白1(URAT1),抑制尿酸重吸收,促进尿酸排泄,降低血尿酸水平。 这三者也是《中国痛风诊疗指南》中推荐的一线降尿酸药物。
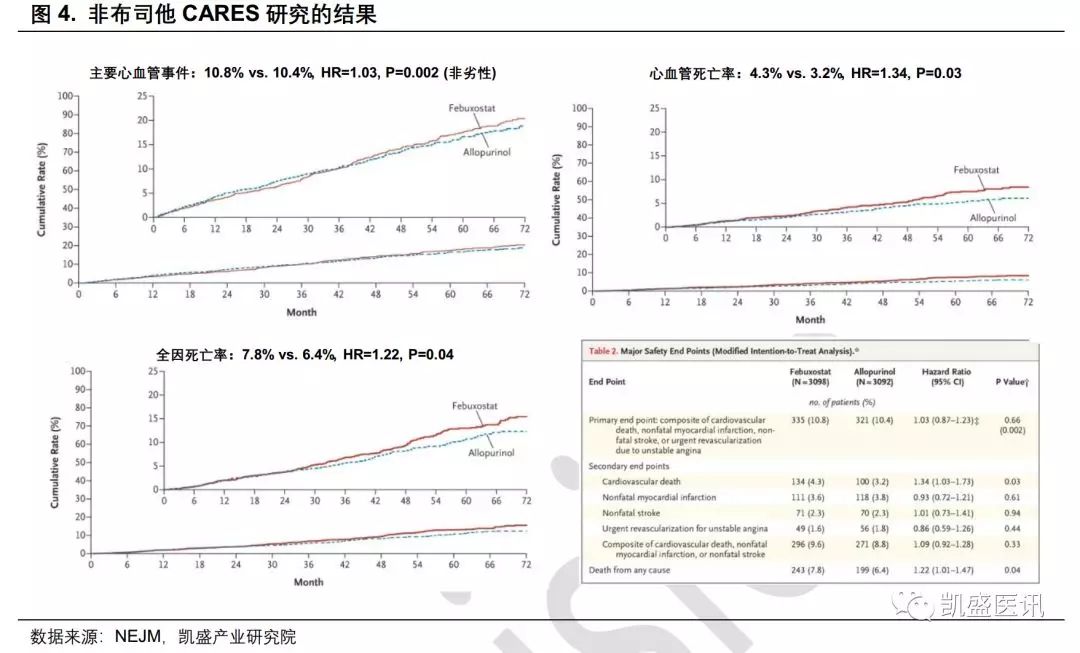
别嘌醇在1966年就被FDA批准,在临床上降尿酸效果显著。但是别嘌醇可引起皮肤过敏反应及肝肾功能损伤,严重者可发生致死性剥脱性皮炎等超敏反应综合征。HLA-B*5801基因阳性和肾功能不全是别嘌醇发生不良反应的危险因素,尤其在中国汉族人群中,HLA-B*5801基因阳性率为6%~8%,而白人仅为2%。 因此在使用别嘌醇前,应该进行HLA-B*5801基因检测,结果阳性的患者禁止使用。此外,也有超过50%的患者在使用别嘌醇后达不到降低血清尿酸 (sUA) 水平的目标。 非布司他为新一代黄嘌呤氧化酶(XO)抑制剂,于2009年获FDA批准上市,并于2013进入中国市场。相较于别嘌醇,非布司他不含嘌呤环,对XO具有更高活性,抑制作用时间较长,降尿酸能力较别嘌醇强而持久;同时别嘌醇对XO 之外的酶还会产生影响,不良反应众多,而非布司他对XO的高度选择性则降低了不良反应的风险。 FACT 研究和APEX证明了非布司他降低血尿酸的效果优于别嘌醇,且进一步CONFIRMS研究证明了,在轻、中度肾功能不全(慢性肾脏病1~3 期)的患者中,非布司他降尿酸的效果及安全性也优于别嘌醇。 虽然非布司他在肾脏安全性上优于别嘌醇,但是临床中非布司他也表现出会增加不良心血管CV 事件风险,因此FDA在2017年11月发布了非布司他心脏相关性死亡风险警告。 2018年3月,《新英格兰》杂志上公布了非布司他CARES 研究的结果,虽然在主要心血管事件(MACE)上达到了非劣性(HR=1.03,P=0.002),但是在心血管死亡风险上显著高于别嘌醇(HR 1.34, p=0.03),全因死亡率也显著提高(HR 1.22, p=0.04)。 FDA也因此给非布司他添加了增加使用者CV死亡及全因死亡率的黑框警告,且建议非布司他在别嘌呤醇治疗失败或不耐受别嘌呤醇的患者中作为二线使用,在服药时应监测心肌梗死和脑卒中的症状和体征。
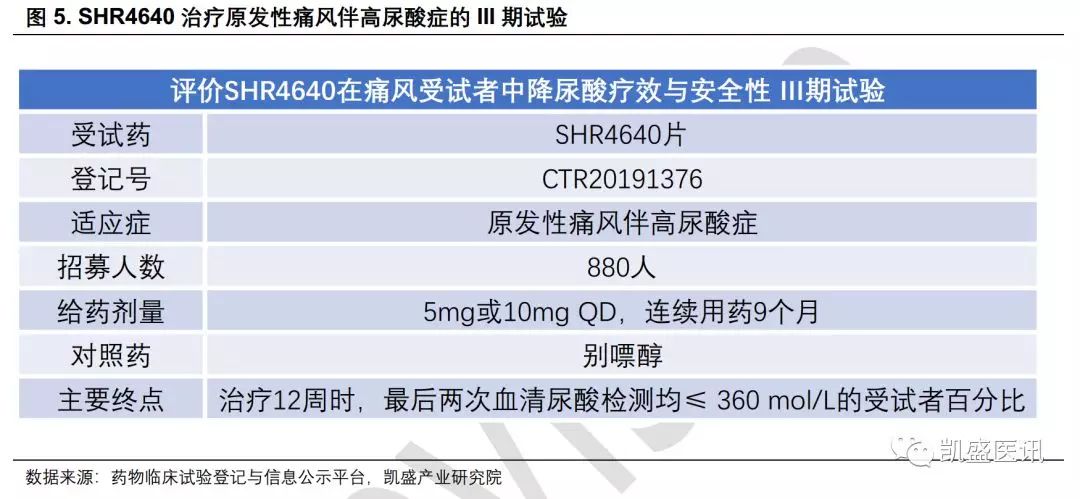
苯溴马隆于1967年开始用于痛风降尿酸治疗,是继丙磺舒之后的第二个促进尿酸排泄的药物。苯溴马隆通过抑制尿酸盐转运蛋白1(URAT1),促进尿酸的肾排泄,可以把血尿酸控制在饱和浓度以下,从而减少尿酸盐结晶沉积,降低痛风的发作机率。 相较于别嘌醇和非布司他等黄嘌呤氧化酶抑制剂,苯溴马隆的作用机制更加合理,因为只有20%患者存在尿酸生成过多,其余80%患者均有不同程度的肾脏排泄不足。 在我国台湾,72%的痛风患者首选苯溴马隆治疗,中国痛风诊疗指南也将其为一线降酸药物,但在欧美痛风指南中仅被列为二线降酸药物。这主要是由于苯溴马隆可能存在潜在的肝脏毒性。苯溴马隆主要在肝脏代谢,通过肝细胞进行转化,这有可能是其肝毒性的原因。 2003年苯溴马隆曾因肝毒性退出欧洲市场,但在2004年又在一些国家重新注册,FDA也未批准其上市。在2004年,国家药品监督管理局也曾警示苯溴马隆的肝损害风险。 因此现有的降尿酸产品在疗效和安全性上都存在一定的局限性,仍需要更加安全有效的产品。以恒瑞SHR4640为代表的新一代URAT1的选择性抑制剂正处于研发之中。 SHR4640已启动III期临床,有成为‘Best in class’的潜力 恒瑞SHR4640片属于新一代URAT1的选择性抑制剂,于2017年5月启动国内Ⅱ期临床试验,并于近日开启Ⅲ期临床试验(CTR20191376),是目前这一领域国内研发进度最快的药物。 初步结果显示,SHR4640单次给予20mg剂量,多次给予10mg剂量下耐受性良好,没有出现严重的不良事件。连续7天给药,尿酸下降约20~55%。 本次III期适应症为原发性痛风伴高尿酸症,试验计划招募880名患者,将与别嘌醇做头对头的比较,试验主要终点为治疗12周时,最后两次血清尿酸检测均≤ 360 mol/L的受试者百分比。
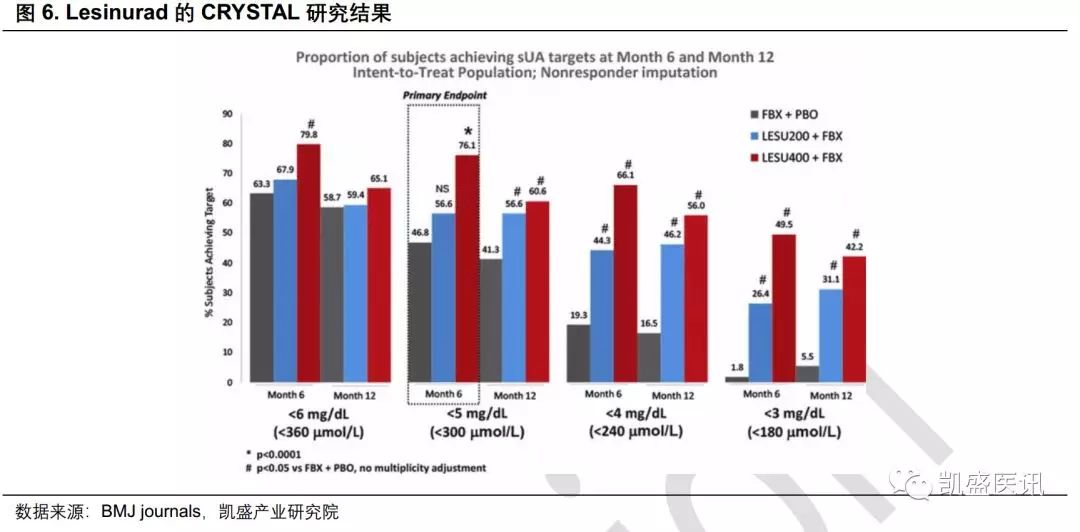
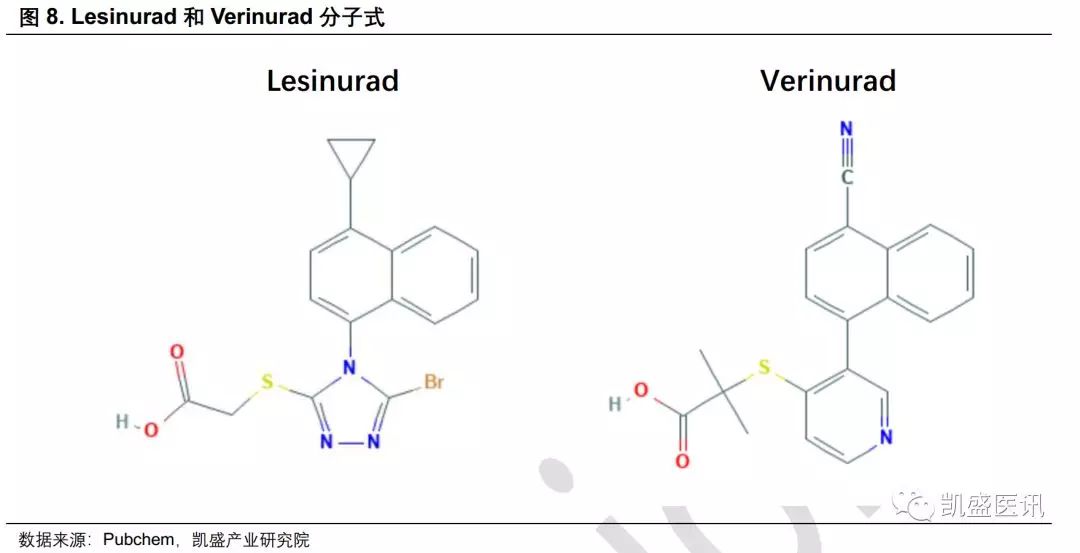
在2015年FDA批准了阿斯利康的Lesinurad上市,这是首个获批的选择性URAT1抑制剂。但是其获批的适应症仅为,200mg剂量与黄嘌呤氧化酶抑制剂联用,治疗黄嘌呤氧化酶抑制剂单药治疗后血清尿酸水平控制不佳的与痛风关联的高尿酸血症。 III期CRYSTAL临床结果显示,400mg剂量Lesinurad+非布司他相较于非布司他单药,能够显著降低患者的血清尿酸(sUA)水平;但是在此剂量时,Lesinurad的肾脏毒性显著,FDA也添加了肾衰的黑框警告。因此阿斯利康仅选择提交了Lesinurad的200mg剂量,但是200mg剂量的效果并不好,未达到6个月sUA水平下降的主要终点。正因为Lesinurad的肾脏毒性和不佳的疗效,其销售惨淡,18年的销售额仅为630万美元。
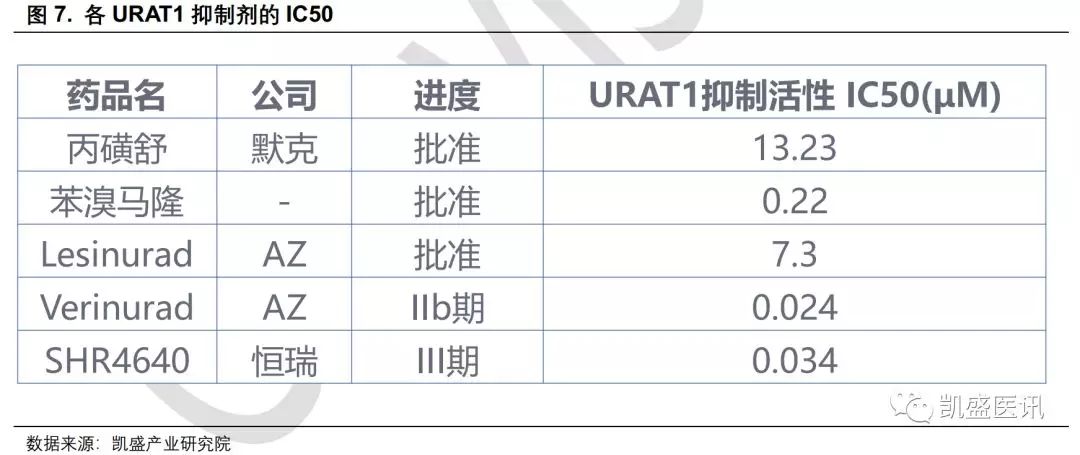
SHR4640有着优于Lesinurad的潜力。 由于Lesinurad对于URAT1的IC50仅为7.3μM,因此使用剂量较大(200mg),可能造成的副作用也较大;而SHR4640抑制URAT1的活性更强,IC50为0.034μM,临床上使用的剂量也仅为5mg/10mg,因此SHR4640有望取得更好的疗效与更低的副反应。
此外,阿斯利康也在Lesinurad的基础上研发了第二代抑制剂Verinurad,大大提高了其对URAT1的抑制活性,IC50为0.024μM。Verinurad目前正在进行慢性肾病的IIb期临床。 已公布的临床结果显示,Verinurad与别嘌醇/非布司他联用降低血尿酸的效果优于别嘌醇/非布司他单药,显示出了很好的潜力。
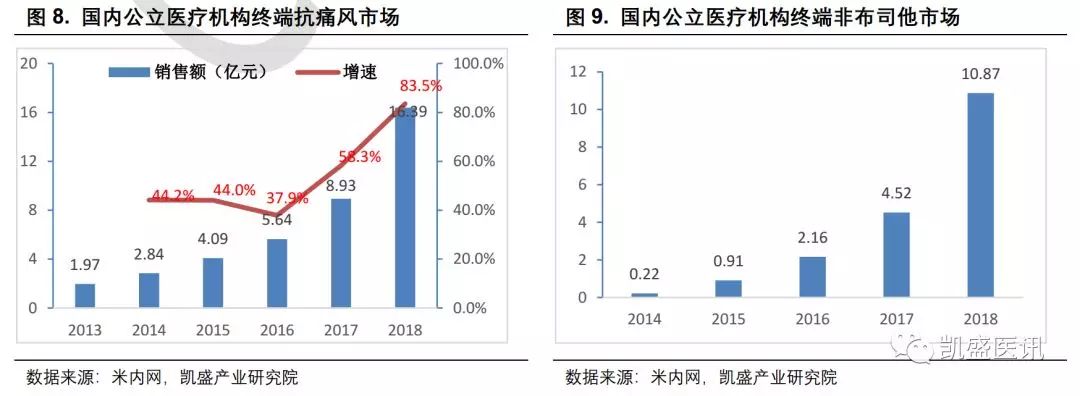
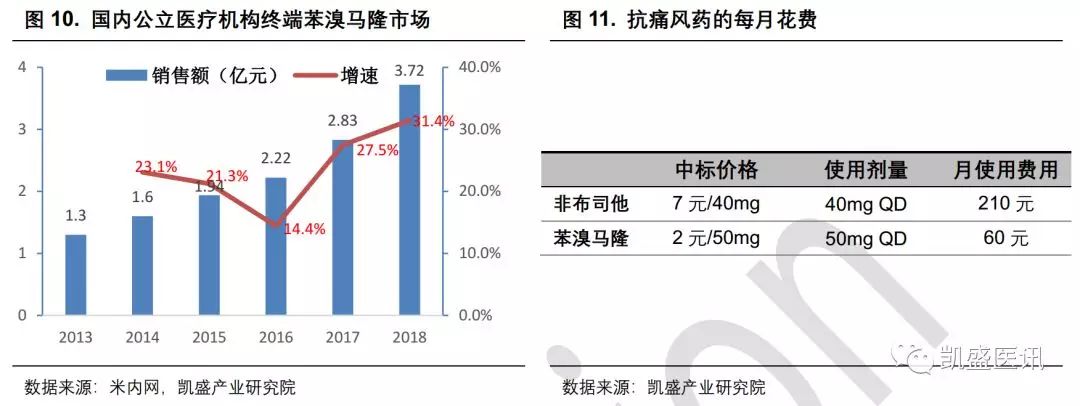
目前国内在研的选择性URAT1抑制剂还有益方生物的D-0120,成都海创药业的HP501和上海璎黎药业的YL-90148,但都还处于早期临床I期。 恒瑞SHR4640进度领先,且有望取得更优异的疗效与安全性,如果最终能获批上市,将在国内的抗尿酸市场占据先发优势。 国内痛风市场高速增长,有望达50亿元规模 目前国内痛风市场保持高速增长,据米内网数据显示,2018年中国公立医疗机构终端抗痛风市场规模达到了16.39亿元,同比增长83.55%。其中非布司他增长更为迅猛,近三年的增长速度均超过100%,其2018年的销售额达到了10.8亿。 非布司他于2017年进入国家医保目录,目前有恒瑞医药、万邦医药和朱养心药业三家仿制药上市销售,而原研药于2018年9月才获得国家药监局批准上市。市场上恒瑞医药和万邦医药的份额约在40%左右,朱养心药业在20%。 目前非布司他的中标价约为7元/40mg,以每日40mg的用量计算,一个月的花费大约在210元。
苯溴马隆也保持着较高的增长率,其2018年终端销售额约为3.72亿元,同比增长31.6%。其中原研药立加利仙占据58%的市场份额,东阳光药的尔同舒占比约为24.5%。苯溴马隆被纳入了国家医保目录2017版,目前的中标价约为2元/50mg,以每日50mg的用量计算,一个月的花费在60元左右。
由以上数据推算得到2018年接受抗痛风药物治疗的患者约在95万人,假设目前痛风患者有2000万人,且每年以5%的速度增长,最终达到10%的治疗渗透率,则整个痛风市场有望在2024年达到50亿元。恒瑞通过其非布司他+SHR4640的布局,将在痛风市场中将分得一大块蛋糕。 转载声明:本文经「凯盛医讯」授权转载。原文题目:《凯盛医药创新药主题研究丨恒瑞SHR4640启动临床III期,进军国内痛风和降尿酸市场》
|
【本文地址】
 返回搜狐,查看更多
返回搜狐,查看更多