| 实验 苯甲酸乙酯的制备 | 您所在的位置:网站首页 › 苯甲酸乙酯的制备实验 › 实验 苯甲酸乙酯的制备 |
实验 苯甲酸乙酯的制备
|
实验 苯甲酸乙酯的制备
时间:2024.5.2
实验 苯甲酸乙酯的制备 一、实验目的: 1、掌握酯化反应原理,苯甲酸乙酯的制备方法,了解三元共沸除水原理。 2、复习分水器的使用及液体有机化合物的精制方法。 3、进一步练习蒸馏、萃取、干燥和折光率的测定等基本操作。 二、实验原理: 苯甲酸,乙醇在浓硫酸的催化下进行酯化反应,生成苯甲酸乙酯与水。
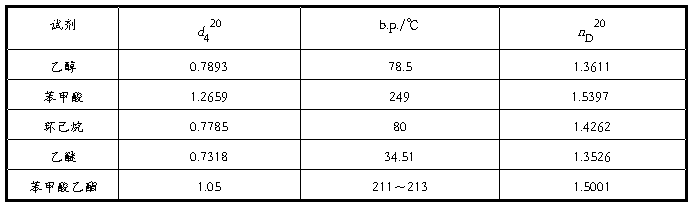
由于苯甲酸乙酯的沸点较高,很难蒸出,所以本实验采用加入环己烷的方法,使环己烷、乙醇和水形成三元共沸物,其沸点为62.1℃。三元共沸物经过冷却形成两相,使环己烷在上层的比例大,再回反应瓶,而水在下层的比例大,放出下层即可除去反应生成的水,使平衡向正方向移动。 三、实验仪器及试剂: 仪器:圆底烧瓶、回流冷凝器、分液漏斗、锥形瓶、烧杯、温度计、球形冷凝管、分水器。 试剂:苯甲酸 4g、无水乙醇10ml、浓硫酸 3ml、Na2CO3、环己烷8ml、乙醚、无水MgSO4、沸石。 装置图:
四、实验步骤: 1、加料:于50ml圆底烧瓶中加入:4g苯甲酸;10ml乙醇;8ml环己烷;3ml浓硫酸,摇匀,加沸石。按照实验仪器左图组装好仪器(安装分水器),加热反应瓶,开始回流。 2、分水回流:开始时回流要慢,随着回流的进行,分水器中出现上下两层。当下层接近分水器支管时将下层液体放入量筒中。继续蒸馏,蒸出过量的乙醇和环己烷,至瓶内有白烟或回流下来液体无滴状(约2h),停止加热。 3、中和:将反应液倒入盛有30mL水的烧杯中,分批加入碳酸钠粉末至溶液呈中性(或弱碱性),无二氧化碳逸出,用PH试纸检验。 4、分离萃取、干燥、蒸馏:用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有几层。用无水MgSO4干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,用牛角管直接接收210~213℃的馏分。 5、检验鉴定: 物理方法:取少量样品,用手扇动其,在闻其气味,应该稍有水果气味。 化学方法:酯与羟胺反应生成一种氧酸。氧酸与铁离子形成牢固的品红色的络合物。在试管中加入两滴新制备的酯,再加入5滴溴水。有溴水的颜色不变或没有白色沉淀生成,将5滴新制备的酯滴入干燥的试管中,在加入7滴3%的盐酸羟胺的95%酒精溶液和3滴2%的NaOH溶液,摇匀后滴入7滴5%HCl溶液和1滴5% FeCl3溶液,试管内显示品红色,证明酯的存在。 色谱分析:查找相关苯甲酸乙酯的色谱图,在分析产品的色谱与之对照。可以证明苯甲酸乙酯存在与否。 五、实验记录及处理: 所加试剂的量: 收集到产品的量: 参考:苯甲酸质量m1=4g 摩尔质量 M1=122g/mol 产物苯甲酸乙酯摩尔质量 M2=150g/mol 实验中乙醇原料过量,苯甲酸设为完全反应,则理论苯甲酸乙酯产物量为 m产物=4 x 150/122 g=4.918g ρ产物=1.046g/ml V理论= m产物÷ρ产物=4.918÷1.046=4.7ml V实际=2.5ml 产率= V实际÷V理论=2.5÷4.7=53.2% 误差分析:①开始分流是没调节好温度,使蒸汽流至蒸馏烧瓶下端管内。②萃取是不慎将试液流出,使产物减少。 六、思考与讨论: 1、本实验采用何种措施提高酯的产率? 2、为什么采用分水器除水? 3、何种原料过量?为什么?为什么要加苯? 4、浓硫酸的作用是什么?常用酯化反应的催化剂有哪些? 5、为什么用水浴加热回流? 6、在萃取和分液时,两相之间有时出现絮状物或乳浊液,难以分层,如何解决? 七、注意事项: 1、注意浓硫酸的取用安全。加入浓硫酸应慢加且混合均匀,防止炭化。 2、回流时温度和时间的控制(反应初期小火加热、反应终点的正确判断)。 3、分水回流开始要控制温度,控制先前一个小时保持回流蒸汽在分水器接圆底烧瓶内管处。 第二篇:实验__苯甲酸乙酯的制备实验 苯甲酸乙酯的制备 一、实验目的: 1、掌握酯化反应原理,苯甲酸乙酯的制备方法,了解三元共沸除水原理。 2、复习分水器的使用及液体有机化合物的精制方法。 3、进一步练习蒸馏、萃取、干燥和折光率的测定等基本操作。 二、实验原理: 苯甲酸,乙醇在浓硫酸的催化下进行酯化反应,生成苯甲酸乙酯与水。

由于苯甲酸乙酯的沸点较高,很难蒸出,所以本实验采用加入环己烷的方法,使环己烷、乙醇和水形成三元共沸物,其沸点为62.1℃。三元共沸物经过冷却形成两相,使环己烷在上层的比例大,再回反应瓶,而水在下层的比例大,放出下层即可除去反应生成的水,使平衡向正方向移动。 三、实验仪器及试剂: 仪器:圆底烧瓶、回流冷凝器、分液漏斗、锥形瓶、烧杯、温度计、球形冷凝管、分水器。 试剂:苯甲酸 4g、无水乙醇10ml、浓硫酸 3ml、Na2CO3、环己烷8ml、乙醚、无水MgSO4、沸石。 装置图:
四、实验步骤: 1、加料:于50ml圆底烧瓶中加入:4g苯甲酸;10ml乙醇;8ml环己烷;3ml浓硫酸,摇匀,加沸石。按照实验仪器左图组装好仪器(安装分水器),加热反应瓶,开始回流。 2、分水回流:开始时回流要慢,随着回流的进行,分水器中出现上下两层。当下层接近分水器支管时将下层液体放入量筒中。继续蒸馏,蒸出过量的乙醇和环己烷,至瓶内有白烟或回流下来液体无滴状(约2h),停止加热。 3、中和:将反应液倒入盛有30mL水的烧杯中,分批加入碳酸钠粉末至溶液呈中性(或弱碱性),无二氧化碳逸出,用PH试纸检验。 4、分离萃取、干燥、蒸馏:用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有几层。用无水MgSO4干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,用牛角管直接接收210~213℃的馏分。 5、检验鉴定: 物理方法:取少量样品,用手扇动其,在闻其气味,应该稍有水果气味。 化学方法:酯与羟胺反应生成一种氧酸。氧酸与铁离子形成牢固的品红色的络合物。在试管中加入两滴新制备的酯,再加入5滴溴水。有溴水的颜色不变或没有白色沉淀生成,将5滴新制备的酯滴入干燥的试管中,在加入7滴3%的盐酸羟胺的95%酒精溶液和3滴2%的NaOH溶液,摇匀后滴入7滴5%HCl溶液和1滴5% FeCl3溶液,试管内显示品红色,证明酯的存在。 色谱分析:查找相关苯甲酸乙酯的色谱图,在分析产品的色谱与之对照。可以证明苯甲酸乙酯存在与否。 五、实验记录及处理: 所加试剂的量: 收集到产品的量: 参考:苯甲酸质量m1=4g 摩尔质量 M1=122g/mol 产物苯甲酸乙酯摩尔质量 M2=150g/mol 实验中乙醇原料过量,苯甲酸设为完全反应,则理论苯甲酸乙酯产物量为 m产物=4 x 150/122 g=4.918g ρ产物=1.046g/ml V理论= m产物÷ρ产物=4.918÷1.046=4.7ml V实际=2.5ml 产率= V实际÷V理论=2.5÷4.7=53.2% 误差分析:①开始分流是没调节好温度,使蒸汽流至蒸馏烧瓶下端管内。②萃取是不慎将试液流出,使产物减少。 六、思考与讨论: 1、本实验采用何种措施提高酯的产率? 2、为什么采用分水器除水? 3、何种原料过量?为什么?为什么要加苯? 4、浓硫酸的作用是什么?常用酯化反应的催化剂有哪些? 5、为什么用水浴加热回流? 6、在萃取和分液时,两相之间有时出现絮状物或乳浊液,难以分层,如何解决? 七、注意事项: 1、注意浓硫酸的取用安全。加入浓硫酸应慢加且混合均匀,防止炭化。 2、回流时温度和时间的控制(反应初期小火加热、反应终点的正确判断)。 3、分水回流开始要控制温度,控制先前一个小时保持回流蒸汽在分水器接圆底烧瓶内管处。 结果与讨论 1、实验数据记录及处理 苯甲酸质量m1=8g 摩尔质量 M1=122g/mol 产物苯甲酸乙酯摩尔质量 M2=150g/mol 实得产物苯甲酸乙酯7.0 ml 产物为无色透明液体,有芳香气味。 实验中乙醇原料过量,苯甲酸设为完全反应,则理论苯甲酸乙酯产物量为 m产物=8 x 150/122 g=9.836g ρ产物=1.046g/ml V理论= m产物÷ρ产物=9.836÷1.046=9.4ml V实际=7.0ml 产率= V实际÷V理论=7.0÷9.4=74.5% 结果分析:本次实验产率算比较高。 2、造成产率降低的原因分析: ①开始分流时温度没调节好,温度过高使没反应的乙醇和水蒸汽带出了烧瓶落 分水器无法返回参与反应,使产物减少。 ②萃取是不慎造成长物流失,使产物减少。 3、实验成败关键: (1)加入浓硫酸应缓慢加入且混合均匀,防止炭化。 (2)要控制好开始回流时候的温度和时间。 (3)中和酸要恰好在中性最好,溶液呈碱性会使产物苯甲酸乙酯部分水解,造成 产 率降低。 更多相关推荐: 苯甲酸乙酯的制备实验报告苯甲酸乙酯的制备班级姓名学号摘要苯甲酸乙酯C9H10O2为无色透明液体其能与乙醇乙醚环己烷混溶不溶于水用于配制香水香精和人造精油等本实验将用苯甲酸酯化制取苯甲酸乙酯再取适量样品做鉴定实验关键词苯甲酸乙酯的制备酯... 苯甲酸乙酯的制备 完整版内含(实验数据处理、思考题)实验苯甲酸乙酯的制备化工104谭锡森33一摘要苯甲酸乙酯C9H10O2无色透明液体能与乙醇乙醚混溶不溶于水用于配制香水香精和人造精油本实验将用苯甲酸酯化制取苯甲酸乙酯再取适量样品做鉴定实验关键词苯甲酸苯甲酸乙酯... 苯甲酸乙酯的制备实验报告苯甲酸乙酯的制备高分子11309苯甲酸乙酯C9H10O2稍有水果气味用于配制香水香精和人造精油也大量用于食品中也可用作有机合成中间体溶剂如纤维素酯纤维素醚树脂等本实验利用酯化反应法制备直接从苯甲酸苯甲酸乙酯再利... 苯甲酸乙酯的合成_实验报告有机化学实验报告20##年11月8日第一部分:实验预习部分一、实验目的(要求)1.学习苯甲酸乙酯的制备原理及操作方法。2.了解共沸蒸馏的基本原理,掌握分水器和旋转蒸发仪的使用方法。3.掌握减压蒸馏的操作方法,进… 对氨基苯甲酸乙酯的制备大实验报告前言对氨基苯甲酸乙酯别名苯佐卡因白色晶体状粉末无嗅无味分子量16519熔点9192易溶于醇醚氯仿能溶于杏仁油橄榄油稀酸难溶于水其作用1紫外线吸收剂主要用于防晒类和晒黑类化妆品对光和空气的化学性稳定对皮肤安全还具... 苯甲酸乙酯的制备预习报告苯甲酸乙酯的制备高分子11309摘要苯甲酸乙酯C9H10O2无色透明液体能与乙醇乙醚混溶不溶于水用于配制香水香精和人造精油本实验将用苯甲酸酯化制取苯甲酸乙酯再取适量样品做鉴定实验关键词苯甲酸乙醇苯甲酸乙酯酯化反... 苏州大学有机化学实验-苯甲酸乙酯的制备苏州大学材料与化学化工学部课程教案实验名称苯甲酸乙酯的制备教学目标学习酯化反应合成苯甲酸乙酯的原理和方法了解共沸除水的原理学习分水器的使用巩固回流减压蒸馏等基本操作教学重点共沸蒸馏技术减压蒸馏技术教学难点减压蒸... 苯甲酸乙酯的制备苯甲酸乙酯的制备化工104班李德昌23号摘要苯甲酸乙酯C9H10O2无色透明液体能与乙醇乙醚混溶不溶于水用于配制香水香精和人造精油本实验将用苯甲酸酯化制取苯甲酸乙酯再取适量样品做鉴定实验关键词苯甲酸苯甲酸乙酯酯... 乙酰水杨酸的制备实验报告乙酰水杨酸阿司匹林的合成实验报告一教学要求1通过本实验了解乙酰水杨酸阿斯匹林的制备原理和方法2进一步熟悉重结晶熔点测定抽滤等基本操作3了解乙酰水杨酸的应用价值二预习内容1重结晶操作2抽虑操作三实验操作流程水杨酸... 苯佐卡因的制备(综合实验报告)订一订beforeexperiment14 苯佐卡因实验报告三:对氨基苯甲酸乙酯的制备(还原)苯佐卡因实验报告三对氨基苯甲酸乙酯的制备还原对氨基苯甲酸乙酯的制备还原实验目的1通过苯佐卡因的合成了解药物合成的基本过程2掌握氧化酯化和还原反应的原理及基本操作3学习以对甲苯胺为原料经乙酰化氧化酸性水解和酯化制... 苯佐卡因实验报告二:对硝基苯甲酸乙酯的制备(酯化)苯佐卡因实验报告二对硝基苯甲酸乙酯的制备酯化对硝基苯甲酸乙酯的制备一实验目的1掌握利用对硝基苯甲酸制备对硝基苯甲酸乙酯的原理及方法2熟练掌握回流抽滤重结晶干燥等过程的操作3练习并掌握酯的纯化方法二实验原理NO2... 苯甲酸乙酯的制备实验报告(18篇) |
【本文地址】
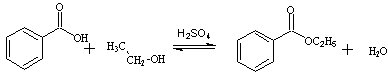
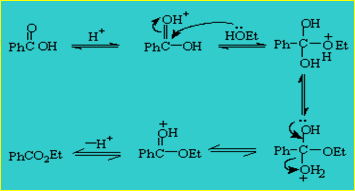 反应机理:
反应机理: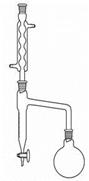 反应装置
反应装置 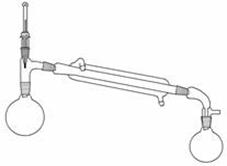 蒸馏装置
蒸馏装置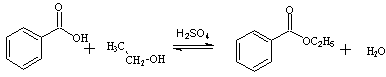
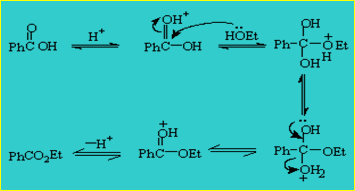 反应机理:
反应机理: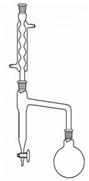 反应装置
反应装置 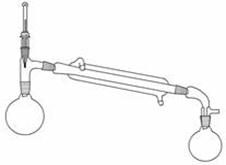 蒸馏装置
蒸馏装置