| m1A多篇齐发:除了m6A,还有哪些热门RNA修饰? | 您所在的位置:网站首页 › mrna转录后 › m1A多篇齐发:除了m6A,还有哪些热门RNA修饰? |
m1A多篇齐发:除了m6A,还有哪些热门RNA修饰?
RNA修饰是表观遗传学中调控转录后基因表达的关键过程,目前对m6A RNA甲基化的研究已进行的如火如荼,但除了m6A以外仍有多种热门RNA修饰类型参与调控转录后的基因表达,其中包括m1A、m5C、m7G、2’-O-甲基化修饰以及ac4C乙酰化修饰,在这些领域的研究极具潜力,近期不断有高影响因子文章的出现(如表1)。云序生物是国内RNA修饰测序的先驱,可针对mRNA和各种非编码RNA提供各类RNA修饰测序服务 (m6A﹑m1A﹑m5C﹑m7G﹑ac4C﹑2’-O-甲基化等)。目前,云序已累计支持客户发表25篇高水平文章,合计影响因子171.6分,是国内支持发文较多、累计影响因子较高的公司。
在m1A领域,云序生物是国内一家有文献发表的测序服务平台。2020年8月,云序客户在Plant physiology发表了矮牵牛m1A甲基化修饰文章,其中的m1A测序和相关数据分析均由云序提供。这个新领域的研究进展如何?有哪些新型的方法思路值得我们借鉴呢?小编汇集了近期多篇m1A修饰文章,带大家把握这一领域的前沿进展。
 表1:近期RNA修饰文章列表
文章展示
1.m1A——矮牵牛mRNA中m1A修饰的动态变化(云序客户文章)
发表期刊:Plant physiology
影响因子:8.005
发表时间:2020.08
实验方法:m1A -seq
文章链接:The N1-Methyladenosine Methylome of Petunia mRNA
N1-Methyladenosine是一种独特的碱基甲基化,因为它阻止了沃森-克里克碱基对,并引入了一个正电荷。m1A在酵母和哺乳动物mRNA中普遍存在,并发挥功能性作用。然而,对于这种修饰在植物mRNA中的丰度、动态和拓扑结构知之甚少。本文通过免疫印迹和液相色谱串联质谱分析了植物生长发育研究的模式植物——矮牵牛花中不同组织和不同发育阶段m1A mRNA修饰的动态模式。通过m1A mRNA的免疫沉淀,我们对矮牵牛mRNA中的m1A进行了全转录谱分析,随后通过m1A -seq(云序提供本次服务),在矮牵牛花冠的3231个基因中发现了4993个m1A峰,其中有251个m1A峰中的A残基部分被胸腺嘧啶取代,或在腺嘌呤位点停止逆转录。m1A在编码序列中富集,在起始密码子之后立即出现单峰。在矮牵牛花冠中,乙烯处理上调了375 mRNA中的400个m1A峰,下调了530 mRNA中的603个m1A峰;*在对照处理的花冠中检测到975个m1A峰,在乙烯处理的花冠中检测到430个m1A峰。沉默矮牵牛tRNA特异性甲基转移酶61A (PhTRMT61A)在体内和体外降低了mRNA中m1A的水平。此外,PhTRMT61A沉默导致叶片发育异常,PhTRMT61A蛋白被定位到细胞核。因此,m1A在mRNA中是一个重要的表观转录组标记,在植物生长发育中发挥作用。
表1:近期RNA修饰文章列表
文章展示
1.m1A——矮牵牛mRNA中m1A修饰的动态变化(云序客户文章)
发表期刊:Plant physiology
影响因子:8.005
发表时间:2020.08
实验方法:m1A -seq
文章链接:The N1-Methyladenosine Methylome of Petunia mRNA
N1-Methyladenosine是一种独特的碱基甲基化,因为它阻止了沃森-克里克碱基对,并引入了一个正电荷。m1A在酵母和哺乳动物mRNA中普遍存在,并发挥功能性作用。然而,对于这种修饰在植物mRNA中的丰度、动态和拓扑结构知之甚少。本文通过免疫印迹和液相色谱串联质谱分析了植物生长发育研究的模式植物——矮牵牛花中不同组织和不同发育阶段m1A mRNA修饰的动态模式。通过m1A mRNA的免疫沉淀,我们对矮牵牛mRNA中的m1A进行了全转录谱分析,随后通过m1A -seq(云序提供本次服务),在矮牵牛花冠的3231个基因中发现了4993个m1A峰,其中有251个m1A峰中的A残基部分被胸腺嘧啶取代,或在腺嘌呤位点停止逆转录。m1A在编码序列中富集,在起始密码子之后立即出现单峰。在矮牵牛花冠中,乙烯处理上调了375 mRNA中的400个m1A峰,下调了530 mRNA中的603个m1A峰;*在对照处理的花冠中检测到975个m1A峰,在乙烯处理的花冠中检测到430个m1A峰。沉默矮牵牛tRNA特异性甲基转移酶61A (PhTRMT61A)在体内和体外降低了mRNA中m1A的水平。此外,PhTRMT61A沉默导致叶片发育异常,PhTRMT61A蛋白被定位到细胞核。因此,m1A在mRNA中是一个重要的表观转录组标记,在植物生长发育中发挥作用。
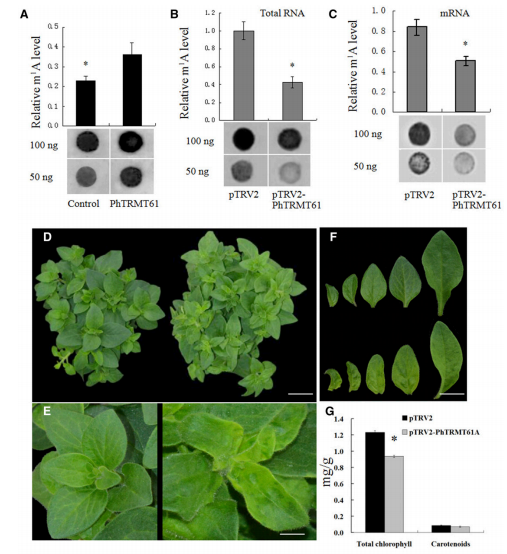 图例1:沉默m1A甲基转移酶PhTRMT61A会导致表型改变
2.对不同RNA修饰调控作用的新见解:重新定义转录和翻译之间的桥梁
发表期刊:Molecular Cancer
影响因子:41.44
发表时间:2020.04.17
文章链接:Novel insight into the regulatory roles of diverse RNA modifications: Re-defining the bridge between transcription and Translation
RNA修饰可以被催化必要反应的各种酶添加或去除,这些修饰在基本的分子机制中发挥作用。mRNA上常见的修饰包括N6-methyladenosine (m6A), N1-methyladenosine (m1A), 5-methylcytosine (m5C), 5-hydroxymethylcytosine (hm5C),假尿苷(Ψ),肌苷(I),尿苷(U)和ribosemethylation(2’-O-Me)。在真核细胞中,这些修饰大部分参与了pre-mRNA剪接、核输出、转录体稳定性和翻译起始。RNA修饰通过参与多种生理过程,在**和非**疾病的发病过程中也发挥调节作用。本文讨论了RNA修饰的生理作用,并将这些作用与疾病发病机制联系起来。作为转录和翻译之间的桥梁,RNA修饰对许多疾病的进展至关重要,甚至可以调节*细胞的命运。
图例1:沉默m1A甲基转移酶PhTRMT61A会导致表型改变
2.对不同RNA修饰调控作用的新见解:重新定义转录和翻译之间的桥梁
发表期刊:Molecular Cancer
影响因子:41.44
发表时间:2020.04.17
文章链接:Novel insight into the regulatory roles of diverse RNA modifications: Re-defining the bridge between transcription and Translation
RNA修饰可以被催化必要反应的各种酶添加或去除,这些修饰在基本的分子机制中发挥作用。mRNA上常见的修饰包括N6-methyladenosine (m6A), N1-methyladenosine (m1A), 5-methylcytosine (m5C), 5-hydroxymethylcytosine (hm5C),假尿苷(Ψ),肌苷(I),尿苷(U)和ribosemethylation(2’-O-Me)。在真核细胞中,这些修饰大部分参与了pre-mRNA剪接、核输出、转录体稳定性和翻译起始。RNA修饰通过参与多种生理过程,在**和非**疾病的发病过程中也发挥调节作用。本文讨论了RNA修饰的生理作用,并将这些作用与疾病发病机制联系起来。作为转录和翻译之间的桥梁,RNA修饰对许多疾病的进展至关重要,甚至可以调节*细胞的命运。
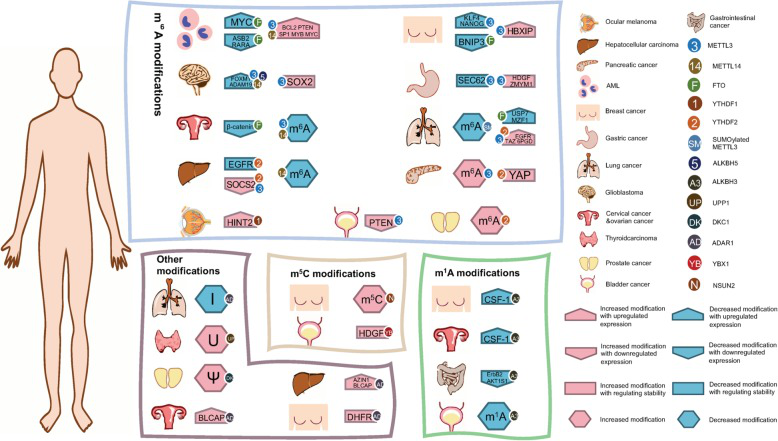 图例2:RNA修饰在发病机制中的调控作用
3.m1A——寡核苷酸质谱法**的应用于体外分析甲基化酶和去甲基化酶
发表期刊:Nucleic Acids Research
影响因子:19.16
发表时间:2020.02.21
文章链接:Broadly applicable oligonucleotide mass spectrometry for the analysis of RNA writers and erasers in vitro
RNA的转录后修饰是通过甲基化酶和去甲基化酶来添加或删除特定的修饰。RNA的质谱(MS)是一种研究寡核苷酸(ON)修饰状态的灵敏度较高的有利工具。文中,作者开发了一种离子配对试剂自由色谱,可用于通过低和高分辨率质谱检测ONs的正离子,且不会干扰到在同一仪器上进行的其他类型的小化合物分析。作者应用ON-MS确定了经RNase T1消化的在体外转录的tRNA的ON。由此产生的tRNAValAAC是人体tRNA ADAT2/3酶的底物并且作者也通过ON-MS在体外证实了肌苷腺苷经脱氨作用生成肌苷以及tRNAValAAC的形成过程。此外,低分辨率的ON-MS被用来在体外监测被细菌AlkB去甲基化的含有m1A修饰的寡核苷酸序列。通过高分辨率的ON-MS检测和匹配被RNase T1消化的tRNA的ONs的修饰水平,证明了高分辨率ON-MS的强大功能。总而言之,本文提出了一种**适用于体外RNA监测寡核苷酸修饰水平的质谱方法。
图例2:RNA修饰在发病机制中的调控作用
3.m1A——寡核苷酸质谱法**的应用于体外分析甲基化酶和去甲基化酶
发表期刊:Nucleic Acids Research
影响因子:19.16
发表时间:2020.02.21
文章链接:Broadly applicable oligonucleotide mass spectrometry for the analysis of RNA writers and erasers in vitro
RNA的转录后修饰是通过甲基化酶和去甲基化酶来添加或删除特定的修饰。RNA的质谱(MS)是一种研究寡核苷酸(ON)修饰状态的灵敏度较高的有利工具。文中,作者开发了一种离子配对试剂自由色谱,可用于通过低和高分辨率质谱检测ONs的正离子,且不会干扰到在同一仪器上进行的其他类型的小化合物分析。作者应用ON-MS确定了经RNase T1消化的在体外转录的tRNA的ON。由此产生的tRNAValAAC是人体tRNA ADAT2/3酶的底物并且作者也通过ON-MS在体外证实了肌苷腺苷经脱氨作用生成肌苷以及tRNAValAAC的形成过程。此外,低分辨率的ON-MS被用来在体外监测被细菌AlkB去甲基化的含有m1A修饰的寡核苷酸序列。通过高分辨率的ON-MS检测和匹配被RNase T1消化的tRNA的ONs的修饰水平,证明了高分辨率ON-MS的强大功能。总而言之,本文提出了一种**适用于体外RNA监测寡核苷酸修饰水平的质谱方法。
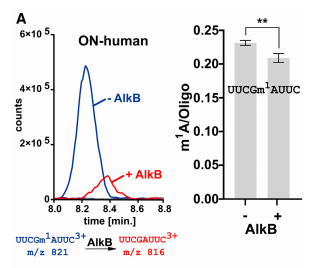 图例3:寡核苷酸的m1A体外检测
4.m1A——确定合适的内源性生物标志物用于健康志愿者多药物和毒素挤压蛋白介导的药物-药物相互作用的风险评
发表期刊:CLINICAL PHARMACOLOGY & THERAPEUTICS
影响因子:6.903
发表时间:2020.04.31
文章链接:Identification of appropriate endogenous biomarker for risk assessment of multidrug and toxin extrusion protein-mediated drug-drug interactions in healthy volunteers
内源性生物标志物的出现促进了药物开发中的临床药物-药物相互作用(DDI)的风险评估。文中对12名健康受试者进行了多药物和**排除蛋白(MATE)抑制剂(10、25和75 mg)交的叉**,以确定合适的内源性生物标志物来评估肾脏中MATE1/2- K介导的DDI。二甲双胍(500mg)作为基准探针药物**MATE1/2-K。除了先前报道的内源性生物标志物候选[肌酐和N1-甲基烟酰胺(1-NMN)], m1A也被纳入为新的生物标志物。由于其肾**率(CLr)的变化以及乙胺嘧啶的剂量与二甲双胍的CLr变化密切相关,因此1-NMN和m1A表现为优良的MATE1/2-K生物标志物。乙胺可降低肌酐的CLr,但其变化与二甲双胍的CLr变化相关性较差。非线性回归分析(CLr vs.血浆中乙胺的平均总浓度)得出了乙胺的抑制常数(Ki)和乙胺敏感性**途径的分数。因此获得的体内Ki值通过使用乙胺的血浆未结合部分进一步转化为未结合Ki,这与MATE1 (1-NMN)和的体外MATE2-K (1-NMN和m1A)的Ki相当。因此,1-NMN和m1A CLr可以作为定量的MATE1/2-K生物标志物来评估健康志愿者的DDI风险。
图例3:寡核苷酸的m1A体外检测
4.m1A——确定合适的内源性生物标志物用于健康志愿者多药物和毒素挤压蛋白介导的药物-药物相互作用的风险评
发表期刊:CLINICAL PHARMACOLOGY & THERAPEUTICS
影响因子:6.903
发表时间:2020.04.31
文章链接:Identification of appropriate endogenous biomarker for risk assessment of multidrug and toxin extrusion protein-mediated drug-drug interactions in healthy volunteers
内源性生物标志物的出现促进了药物开发中的临床药物-药物相互作用(DDI)的风险评估。文中对12名健康受试者进行了多药物和**排除蛋白(MATE)抑制剂(10、25和75 mg)交的叉**,以确定合适的内源性生物标志物来评估肾脏中MATE1/2- K介导的DDI。二甲双胍(500mg)作为基准探针药物**MATE1/2-K。除了先前报道的内源性生物标志物候选[肌酐和N1-甲基烟酰胺(1-NMN)], m1A也被纳入为新的生物标志物。由于其肾**率(CLr)的变化以及乙胺嘧啶的剂量与二甲双胍的CLr变化密切相关,因此1-NMN和m1A表现为优良的MATE1/2-K生物标志物。乙胺可降低肌酐的CLr,但其变化与二甲双胍的CLr变化相关性较差。非线性回归分析(CLr vs.血浆中乙胺的平均总浓度)得出了乙胺的抑制常数(Ki)和乙胺敏感性**途径的分数。因此获得的体内Ki值通过使用乙胺的血浆未结合部分进一步转化为未结合Ki,这与MATE1 (1-NMN)和的体外MATE2-K (1-NMN和m1A)的Ki相当。因此,1-NMN和m1A CLr可以作为定量的MATE1/2-K生物标志物来评估健康志愿者的DDI风险。
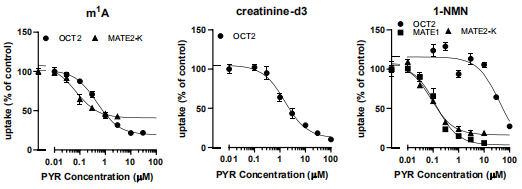 图例4:乙胺对OCT2、MATE1和MATE2-K的影响
云序生物m1A修饰研究五大模块
01 m1A RNA修饰测序
m1A RNA修饰测序(m1A-seq)
对m1A RNA甲基化,目前流行的检测手段为m1A-Seq技术,适用于m1A RNA甲基化谱研究,快速筛选m1A RNA甲基化靶基因。云序可提供mRNA和多种非编码RNA的m1A测序:
√ m1A 全转录组测序(涵盖mRNA,LncRNA,circRNA)
√ m1A LncRNA测序(涵盖LncRNA和mRNA)
√ m1A Pri-miRNA测序(涵盖Pri-miRNA和mRNA)
√ m1A mRNA测序
02 检测整体m1A RNA修饰水平
LC-MS/MS检测整体RNA修饰水平
准确高效,可以实现一次检测,9类修饰水平检测,一步到位。
03 m1A RNA修饰上游酶的筛选
m1A RNA修饰相关酶PCR芯片
寻找上游直接调控m1A RNA甲基化的甲基转移酶。
04 m1A RNA修饰靶基因验证
meRIP-qPCR
云序提供各类不同修饰的meRIP-qPCR服务,可针对mRNA,lncRNA,环状RNA等不同类型的RNA分子进行检测,低通量验证RNA修饰靶基因表达水平。
05机制互作研究
5.1 RIP-seq/qPCR
筛选或验证RNA修饰直接靶点,研究RNA修饰靶基因的调控机制。
5.2 RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
5.3 双荧光素酶实验
图例4:乙胺对OCT2、MATE1和MATE2-K的影响
云序生物m1A修饰研究五大模块
01 m1A RNA修饰测序
m1A RNA修饰测序(m1A-seq)
对m1A RNA甲基化,目前流行的检测手段为m1A-Seq技术,适用于m1A RNA甲基化谱研究,快速筛选m1A RNA甲基化靶基因。云序可提供mRNA和多种非编码RNA的m1A测序:
√ m1A 全转录组测序(涵盖mRNA,LncRNA,circRNA)
√ m1A LncRNA测序(涵盖LncRNA和mRNA)
√ m1A Pri-miRNA测序(涵盖Pri-miRNA和mRNA)
√ m1A mRNA测序
02 检测整体m1A RNA修饰水平
LC-MS/MS检测整体RNA修饰水平
准确高效,可以实现一次检测,9类修饰水平检测,一步到位。
03 m1A RNA修饰上游酶的筛选
m1A RNA修饰相关酶PCR芯片
寻找上游直接调控m1A RNA甲基化的甲基转移酶。
04 m1A RNA修饰靶基因验证
meRIP-qPCR
云序提供各类不同修饰的meRIP-qPCR服务,可针对mRNA,lncRNA,环状RNA等不同类型的RNA分子进行检测,低通量验证RNA修饰靶基因表达水平。
05机制互作研究
5.1 RIP-seq/qPCR
筛选或验证RNA修饰直接靶点,研究RNA修饰靶基因的调控机制。
5.2 RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
5.3 双荧光素酶实验
验证两基因互作,研究相应的分子调控机制。 云序客户RNA修饰文章列表 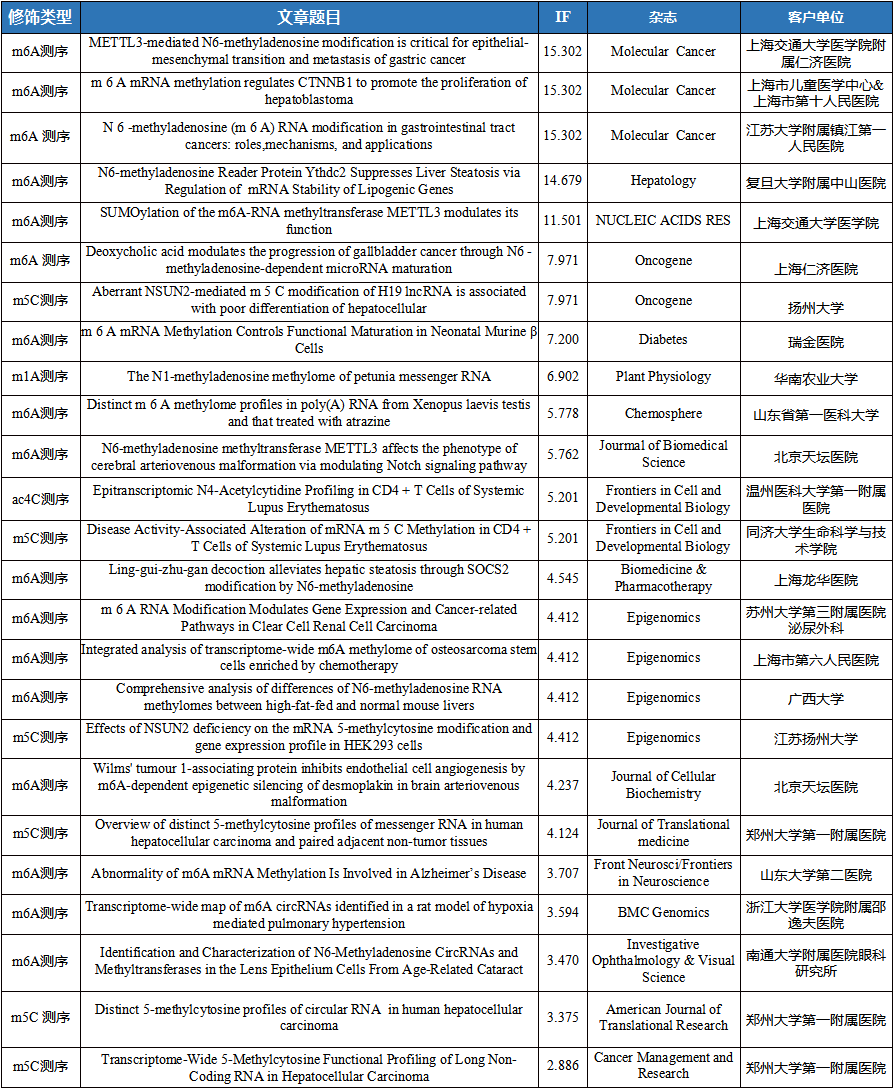 相关产品链接
相关产品链接
m6A RNA甲基化测序 m5C RNA甲基化测序 m7G (m3C)RNA 甲基化测序 2’-O-RNA甲基化测序 ac4C乙酰化测序 比色法检测整体m6A甲基化水平 m6A Writers/Erasers/Readers预制病毒库 RNA修饰相关酶 PCR芯片 ATAC-Seq ChIP-seq eccDNA测序 往期回顾云序客户**成果揭秘:三个月内搞定5分m6A甲基化谱文章? 云序4篇项目文章|m5C RNA修饰表达谱文章教您如何另辟蹊径快速发文 去甲基化酶ALKBH5在胰腺*中的作用荣登15分杂志 人类组织中m6A修饰的动态变化和进化 METTL3调控m6A甲基化修饰影响小鼠脂肪细胞发育云序客户|华南农业大学余义勋课题组揭示植物RNA m1A修饰调控机制 m6A RNA甲基化10+文章就看这篇! Cell Research 新玩法:m6A+circRNA玩转17分文章 m6A阅读器YTHDF1介导EIF3C翻译促进卵巢*进展 RNA甲基化 m6A有望成为不育症**新靶点 云序年终巨献|5篇m6A甲基化文章教你如何纯测序数据 发5分sci何川教授**Science揭秘m6A修饰新功能 -- 调控染色质状态和转录活性 临近年末,恭贺云序客户再发10分RNA甲基化文章
上海云序生物科技有限公司 Shanghai Cloud-seq Biotech Co., Ltd. 地址:上海市松江区莘砖公路 518 号 20 号楼 3 楼 电话:021-64878766 传真:021-64878766 网址:www.cloud-seq.com.cn 邮箱:[email protected]
|
【本文地址】
公司简介
联系我们
