| 碱式碳酸镁[Mg2(OH)2CO3]和过氧化镁都是重要化工原料.Ⅰ 以Mg2(OH)2CO3为原料.制备产品MgO2的步骤如下:2CO3得到三种氧化物.其中一种常温下是气体.且能使澄清石灰水变浑浊.煅烧时反应的化学方程式为 .(2)转化 向所得固体中加双氧水充分搅拌.发生反应MgO+H2O2=MgO2+H2O.温度升高.说明该反应 热量.其他条件相同. 题目和参考答案――青夏教育精英家教网―― | 您所在的位置:网站首页 › mgo2的电子式 › 碱式碳酸镁[Mg2(OH)2CO3]和过氧化镁都是重要化工原料.Ⅰ 以Mg2(OH)2CO3为原料.制备产品MgO2的步骤如下:2CO3得到三种氧化物.其中一种常温下是气体.且能使澄清石灰水变浑浊.煅烧时反应的化学方程式为 .(2)转化 向所得固体中加双氧水充分搅拌.发生反应MgO+H2O2=MgO2+H2O.温度升高.说明该反应 热量.其他条件相同. 题目和参考答案――青夏教育精英家教网―― |
碱式碳酸镁[Mg2(OH)2CO3]和过氧化镁都是重要化工原料.Ⅰ 以Mg2(OH)2CO3为原料.制备产品MgO2的步骤如下:2CO3得到三种氧化物.其中一种常温下是气体.且能使澄清石灰水变浑浊.煅烧时反应的化学方程式为 .(2)转化 向所得固体中加双氧水充分搅拌.发生反应MgO+H2O2=MgO2+H2O.温度升高.说明该反应 热量.其他条件相同. 题目和参考答案――青夏教育精英家教网――
|
碱式碳酸镁[Mg2(OH)2CO3]和过氧化镁(MgO2)都是重要化工原料。 Ⅰ 以Mg2(OH)2CO3为原料,制备产品MgO2的步骤如下: (1)煅烧 煅烧Mg2(OH)2CO3得到三种氧化物,其中一种常温下是气体,且能使澄清石灰水变浑浊。煅烧时反应的化学方程式为 。 (2)转化 向所得固体中加双氧水充分搅拌,发生反应MgO+H2O2=MgO2+H2O。温度升高,说明该反应 热量(填“放出”或“吸收”)。其他条件相同,煅烧温度、煅烧时间不同,所得MgO对MgO2产率(产率=
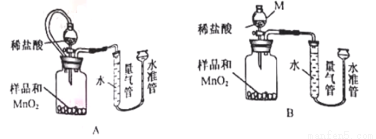
(3)分离 得到产品 (4)测定 假设产品中仅混有少量MnO。某小组设计下列装置,通过测定生成O2的体积,计算MgO2的质量分数。
已知:A.MnO2与稀盐酸不反应 B.MgO2+2HCl=MgCl2+H2O2 C.2MgO2 ①仪器M的名称是 。MnO2的作用是 。 ②相同条件下, 能使测定结果更准确。(填“装置A”或“装置B”) ③实验室用溶质质量分数为37%、密度是1.18g・mL-1的浓盐酸配制10%的稀盐酸110g,需要水 mL。(水的密度是1g・mL-1,计算结果保留一位小数) ④经讨论,该小组又设计了下列3种方案。分别取5.0g产品进行实验,能确定MgO2质量分数的是 。(填序号) A.加热,使MgO2完全分解,测出剩余固体的质量 B.与足量炭粉在高温下充分反应,测出生成Mg的质量 C.先加足量稀盐酸,再加足量NaOH溶液,充分反应,测出Mg(OH)2质量 Ⅱ MgCl2是制备Mg2(OH)2CO3的原料。现用含碳酸镁84%的菱镁矿制备MgCl2,反应如下: MgCO3+Cl2+CO |
【本文地址】
| 今日新闻 |
| 推荐新闻 |
| 专题文章 |
 ×100%)的影响分别如图所示。则最佳的煅烧温度为 ℃,煅烧时间为 小时。
×100%)的影响分别如图所示。则最佳的煅烧温度为 ℃,煅烧时间为 小时。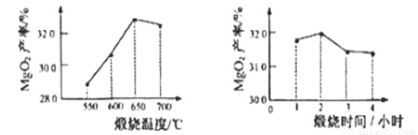
 2MnO+O2↑ D.MgO+C
2MnO+O2↑ D.MgO+C Mg+CO↑
Mg+CO↑